慢性腎臓病における細胞外小胞による臓器間相互作用
文責 萬代 新太郎 Shintaro Mandai
慢性腎臓病(CKD)は腎臓局所の障害にとどまらず、心血管病やサルコペニア、認知機能低下など多臓器に波及する全身疾患である。研究の端緒として、CRISPR/Cas9を一塩基多型(SNP)の機能解析に応用し、高血圧感受性SNP STK39 rs3754777の生物学的意義を解明した(Hypertension 2015)。続いて、腎臓—代謝臓器間の連関に着目し、骨格筋肥大・再生モデルを構築。SPAK/Na–K–Cl共輸送体による骨格筋形成制御、さらにはWNK1キナーゼが筋肥大を惹起することを示し、利尿薬や電解質輸送が筋機能へ及ぼす影響を新たな視点から提示した(Sci Rep 2017, Scie Rep 2018)。
この基盤の上に、細胞外小胞(small extracellular vesicles; EV)を介した細胞間・臓器間コミュニケーションにより、腎臓病が遠隔臓器障害(動脈硬化、サルコペニアなど)を誘導する機序を探究してきた。とくに血中循環EVが内包するmicroRNAが、血管平滑筋細胞の骨芽細胞様形質転換と石灰化を促進することを、治療候補化合物の知見とともに報告した(Circulation Research 2023)。さらに、循環EV microRNAがCKDおよび心血管イベントの予測に資することを、臨床コホート解析で示し最近の成果(Journal of the American Heart Association 2025)や、CKDにおけるEVの役割を総説として整理した(Clin Exp Nephrol 2025)(図)ことは、診断・治療の双方に新機軸を与えるものである。EVを通じた臓器間相互作用の理解は、生体の恒常性維持機構や老化制御に新たな光を当て、CKDの克服のため新たな治療開発に繋がる可能性がある。
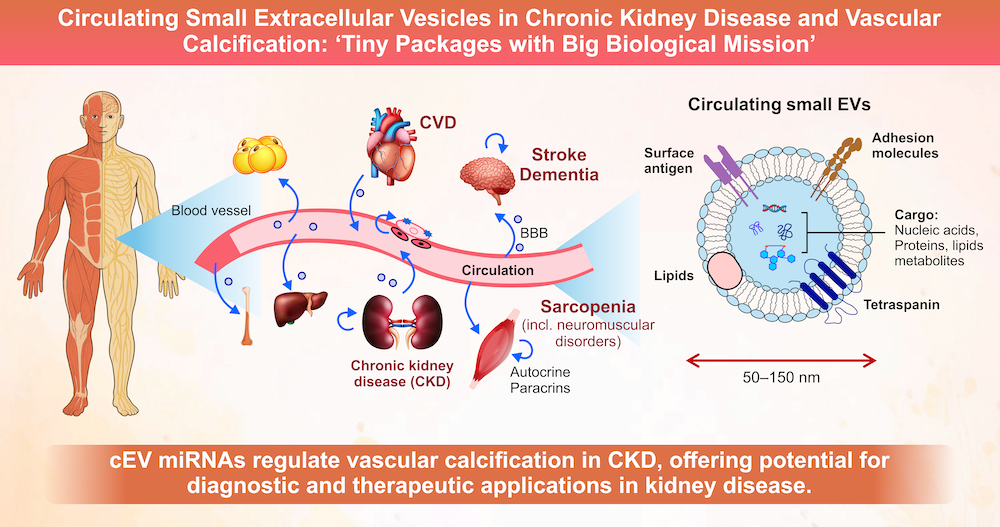
図1. CKDと臓器間相互作用におけるEVの役割(文献2)
EVは50–150 nmの微粒子で、脂質二重膜に包まれ、タンパク質・脂質・核酸などを含み、細胞同士・臓器同士の情報伝達を担う。腎臓、心臓、血管(特に血管内皮、血管平滑筋(VSMC))、骨格筋、脳、骨など多くの臓器に作用し、CKDに伴う多臓器障害や早期老化(“腎性老化”)に関与すると考える。
1. Inaba S, Hasegawa T, Nakano Y, Naito S, Suzukawa R, Koide T, Sekiya H, Matsuki H, Fujiki T, Kikuchi H, Arai Y, Mori Y, Ando F, Mori T, Susa K, Iimori S, Sohara E, Uchida S, Mandai S. Circulating Extracellular Vesicle MicroRNAs as Predictive Biomarkers for Kidney and Cardiovascular Events. Journal of the American Heart Association. 2025. doi: 10.1161/JAHA.125.045148
2. Mandai S. Circulating small extracellular vesicles in chronic kidney disease and vascular calcification: “Tiny packages with big biological mission”. Clinical and Experimental Nephrology. 2025. Online ahead of print. doi: 10.1007/s10157-025-02793-7
3. Koide T, Mandai S, Kitaoka R, Matsuki H, Chiga M, Yamamoto K, Yoshioka K, Yagi Y, Suzuki S, Fujiki T, Ando F, Mori T, Susa K, Iimori S, Naito S, Sohara E, Rai T, Yokota T, Uchida S. Circulating Extracellular Vesicle-Propagated microRNA Signature as a Vascular Calcification Factor in Chronic Kidney Disease. Circulation Research. 2023;132(4):415–431. doi: 10.1161/CIRCRESAHA.122.321939
4. Matsuki H, Mandai S, Shiwaku H, Koide T, Takahashi N, Yanagi T, Inaba S, Ida S, Fujiki T, Mori Y, Ando F, Mori T, Susa K, Iimori S, Sohara E, Takahashi H, Uchida S. Chronic kidney disease causes blood-brain barrier breakdown via urea-activated matrix metalloproteinase-2 and insolubility of tau protein. Aging (Albany NY). 2023;15(20):10972–10995. doi: 10.18632/aging.205164
5. Mandai S, Mori T, Nomura N, Furusho T, Arai Y, Kikuchi H, Sasaki E, Sohara E, Rai T, Uchida S. WNK1 regulates skeletal muscle cell hypertrophy by modulating the nuclear localization and transcriptional activity of FOXO4. Scientific Reports. 2018;8(1):9101. doi: 10.1038/s41598-018-27414-0
6. Mandai S, Furukawa S, Kodaka M, Hata Y, Mori T, Nomura N, Ando F, Mori Y, Takahashi D, Yoshizaki Y, Kasagi Y, Arai Y, Sasaki E, Yoshida S, Furuichi Y, Fujii NL, Sohara E, Rai T, Uchida S. Loop diuretics affect skeletal myoblast differentiation and exercise-induced muscle hypertrophy. Scientific Reports. 2017;7:46369. doi: 10.1038/srep46369
7. Mandai S, Mori T, Sohara E, Rai T, Uchida S. Generation of Hypertension-Associated STK39 Polymorphism Knockin Cell Lines With the CRISPR/Cas9 System. Hypertension. 2015;66(6):1199–1206. doi: 10.1161/HYPERTENSIONAHA.115.05872
