次世代シーケンサー(NGS)による腎臓病遺伝子解析研究
文責 森 崇寧 Takayasu Mori 蘇原 映誠 Eisei Sohara
2010年頃、次世代シーケンサー(NGS, 遺伝子配列を大規模かつ高速に解析する技術)が登場したことでヒト遺伝子解析研究は大きく進展し、腎臓病領域もその例外ではありませんでした。遺伝子検査に対する敷居は以前より格段に下がり,成人の慢性腎臓病(CKD)患者でも積極的に遺伝子検査が実施される時代になりつつあります。
2019年Groopmanらは約3,000名以上のCKD患者に対し全遺伝子(エクソーム)解析を行い、CKD全体の約10%は単一遺伝子疾患であると報告するなど1)、これまで糖尿病,高血圧,慢性糸球体腎炎が主な原因と考えられていたCKDの捉え方にパラダイムシフトが生じました.
森崇寧 講師は国立遺伝学研究所、ワシントン大学Bamshad研究室への留学を経て習熟したNGS解析技術を世界にも先駆けて腎臓病領域に導入し、蘇原映誠 准教授のご指導と協力を得て総計240種類の腎疾患責任遺伝子群を網羅した腎臓病遺伝子診断パネル(SPEEDI-KID, PKDパネル)を構築し2014年から運用を続けています2), 3)。これまでに全国から2,000例以上の解析依頼を受け、創出された原著論文は73本(2025年末時点)、学会発表は100件以上と腎臓遺伝学の進歩に貢献してきました。下記にいくつかの例をご紹介します。
・日本人Gitelman症候群の確定診断例と未解決(臨床診断)例の比較検討により、それぞれの臨床的特徴や日本人ホットスポット変異を明らかにしました4)(Mori T et al. Human Mutat. 2021)。
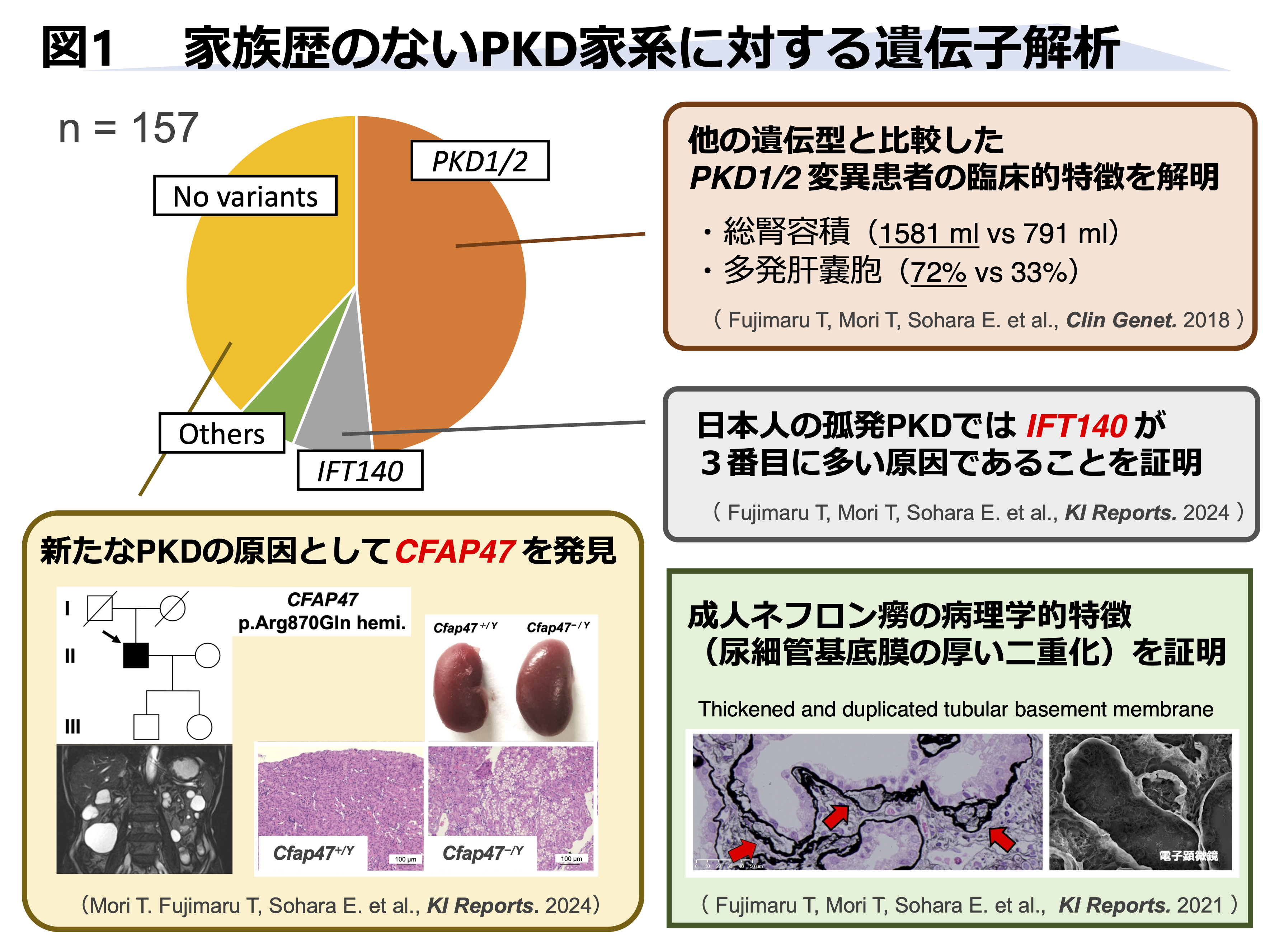
・遺伝性ネフロン癆(NPH)が疑われた18名の患者を対象にパネル遺伝子解析と病理学的評価を行い、NPHの遺伝子背景およびNPHに特異的な病理所見として尿細管基底膜の厚い二重化があることを報告しました5)(Fujimaru T, Sohara E, et al. Kidney Int Rep. 2021)(図1)
・透析導入原疾患不明の日本人血液透析患者90名のパネル遺伝子解析により、約10%に遺伝性腎疾患患者が含まれていることを示しました。この患者群では事前に正しく診断できていた患者はいませんでした6)(Fujimaru T, Mori T, Sohara E, et al. Kidney Int Rep. 2024)(2025年日本透析医学会木本賞受賞論文)。(図2)
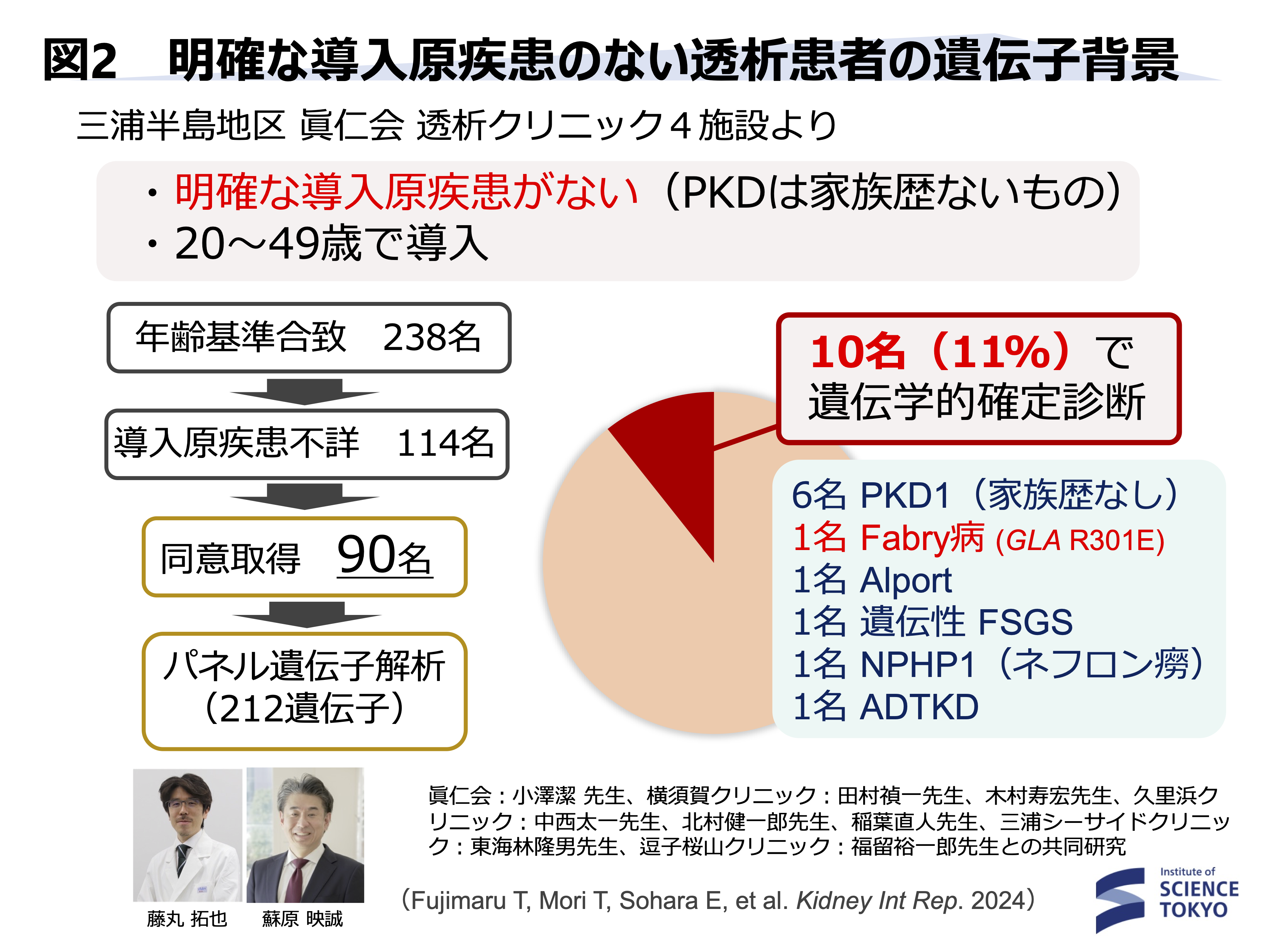
・家族歴のない多発性嚢胞腎患者157人のうち7人(4.5%)はIFT140遺伝子の単一ヘテロ変異が原因であり、PKD1/2に続く第3の原因であることを日本人コホートデータとして初めて報告しました7)(Fujimaru T, Mori T, Sohara E, et al. Kidney Int Rep. 2024)。(図1)
・ワシントン大学との共同研究にて、家族歴のない多発性嚢胞腎患者のうち遺伝学的診断のつかなかった47名の患者を全ゲノムシーケンスすることで、新たな嚢胞原因遺伝子CFAP47を発見しました8)(Mori T, Sohara E, et al. Kidney Int Rep. 2024)。(図1)
・腎臓病家族歴のある患者では41.2%がアルポート症候群であり、学校検診で指摘された血尿は強くアルポート症候群を示唆する(特異度 88%)ことを報告しました9)(Kawamoto R, Mori T, et al. J Nephrol. 2025)(図3)
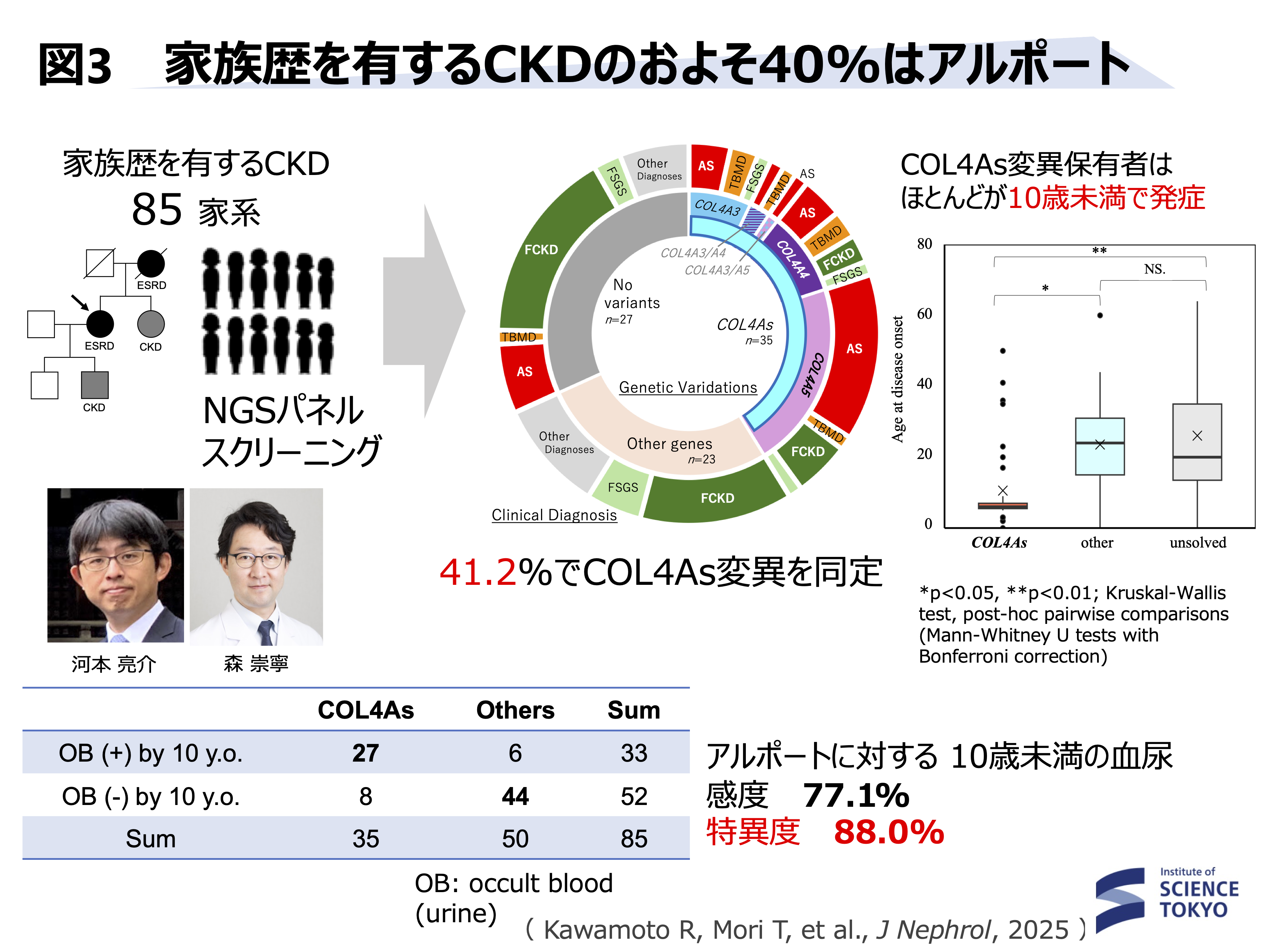
2023年度はクラウドファンディングを開催し、おかげさまで約400名の支援者の方々から2,000万円近いご支援をいただき、皆様方のご支持や高い注目度を物語っておりました。さらに、これまでの膨大な解析データから、日本人CKDに隠れる遺伝性腎疾患を約90%カバーする上位20遺伝子を選定し、既に特許申請を完了(特願2023-177278)、保険収載を目指し、現在企業と共同で日本人に特化したCKDパネル開発を進めています(図4)。また2026年度の「東京都 大学研究者による事業提案制度」に採択され、3年間で2.8億円の総事業費を獲得しました。早期の検査で早期に遺伝性腎疾患患者を見出し、適切な治療策を講じることで一人でも多くの透析患者を減らすよう尽力して参ります。
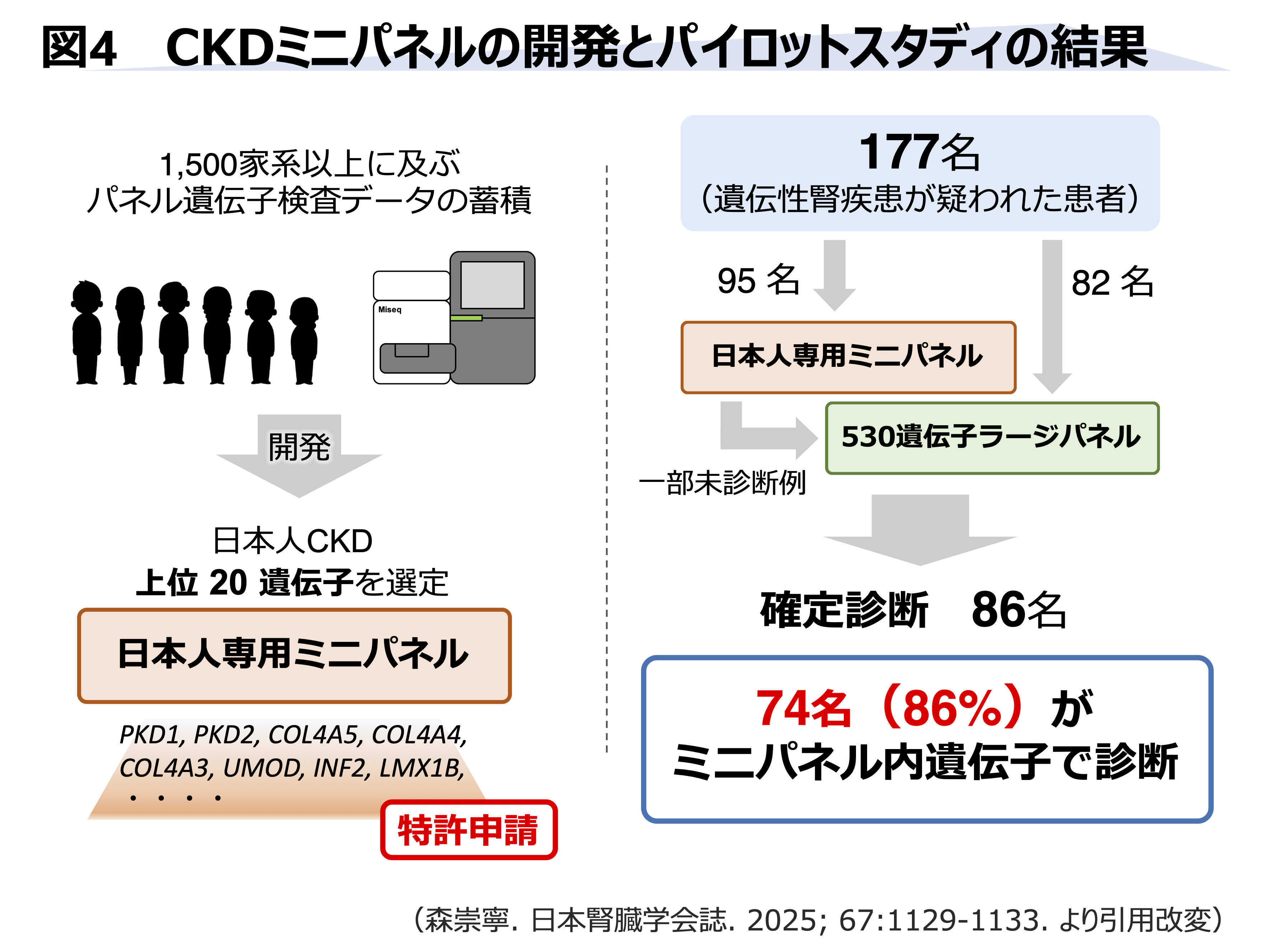
1. Groopman E, Goldstein D, Gharavi A. Diagnostic Utility of Exome Sequencing for Kidney Disease. Reply. N Engl J Med. May 23 2019;380(21):2080-2081. doi:10.1056/NEJMc1903250
2. Mori T, Hosomichi K, Chiga M, et al. Comprehensive genetic testing approach for major inherited kidney diseases, using next-generation sequencing with a custom panel. Clin Exp Nephrol. Feb 2017;21(1):63-75. doi:10.1007/s10157-016-1252-1
3. Fujimaru T, Mori T, Sekine A, et al. Kidney enlargement and multiple liver cyst formation implicate mutations in PKD1/2 in adult sporadic polycystic kidney disease. Clin Genet. Jul 2018;94(1):125-131. doi:10.1111/cge.13249
4. Mori T, Chiga M, Fujimaru T, et al. Phenotypic differences of mutation-negative cases in Gitelman syndrome clinically diagnosed in adulthood. Hum Mutat. Mar 2021;42(3):300-309. doi:10.1002/humu.24159
5. Fujimaru T, Kawanishi K, Mori T, et al. Genetic Background and Clinicopathologic Features of Adult-onset Nephronophthisis. Kidney Int Rep. May 2021;6(5):1346-1354. doi:10.1016/j.ekir.2021.02.005
6. Fujimaru T, Mori T, Chiga M, et al. Genetic Diagnosis of Adult Hemodialysis Patients With Unknown Etiology. Kidney Int Rep. Apr 2024;9(4):994-1004. doi:10.1016/j.ekir.2024.01.027
7. Fujimaru T, Mori T, Sekine A, et al. Importance of. Kidney Int Rep. Sep 2024;9(9):2685-2694. doi:10.1016/j.ekir.2024.06.021
8. Mori T, Fujimaru T, Liu C, et al. CFAP47 is Implicated in X-Linked Polycystic Kidney Disease. Kidney Int Rep. Dec 2024;9(12):3580-3591. doi:10.1016/j.ekir.2024.09.013
9. Kawamoto R, Mori T, Chiga M, et al. Importance of family history and health checkup for school-aged children for type IV collagen-associated nephropathy in hereditary kidney disease. J Nephrol. Sep 2025;38(7):1909-1916. doi:10.1007/s40620-025-02355-w
