WNKキナーゼシグナルの同定と全容解明
執筆担当:森 崇寧,蘇原 映誠
2001年、偽性低アルドステロン症II型(PHAII)という稀な遺伝性高血圧症の原因遺伝子としてWNK1, WNK4の変異が同定されました。内田研究室では世界に先駆けてWNK4変異を導入したPHA2モデルマウスの創出に成功し、腎臓遠位尿細管に発現するNCC(Na-Cl共輸送体)の恒常的活性化が病態メカニズムの本体であることを解明しました。さらにWNKキナーゼの活性は同じセリンスレオニンキナーゼに属するoxidative stress-response protein 1 (OSR1) およびSTE20/SPS1-related proline/alanine-rich kinase (SPAK) を介していることを各種遺伝子改変マウスを用いてin vivoレベルで証明し、「WNK-OSR1/SPAK-NCCシグナルカスケード」という概念を確立しました。その後他のPHAII家系から新たにKLHL3とCullin3 が原因として同定され、その病態メカニズム解析を通して、WNKの分解系による制御が重要な役割を果たしている事も明らかにしました。当教室ではin vivoでの検証という考え方を大切にしながら、生体内の塩出納や血圧調節において重要な役割を果たすWNKシグナル制御機構の全容解明に多大な貢献を果たしました。
1. WNKキナーゼと偽性低アルドステロン症Ⅱ型
2001年に、偽性低アルドステロン症Ⅱ型(Pseudohypoaldosteronism type II : PHAⅡ)という稀な遺伝性疾患の原因遺伝子としてWNK1とWNK4変異が報告されました1)。本症は高血圧、高カリウム血症、高クロール性代謝性アシドーシスを特徴とし、腎遠位尿細管に発現するNCC(Na-Cl 共輸送体)の特異的阻害剤であるサイアザイド利尿薬で、高血圧を含む諸症状が改善することから、NCCの機能亢進が病態の主座であると考えられていましたが、当時WNKキナーゼとNCC活性との関連性は不明でした。
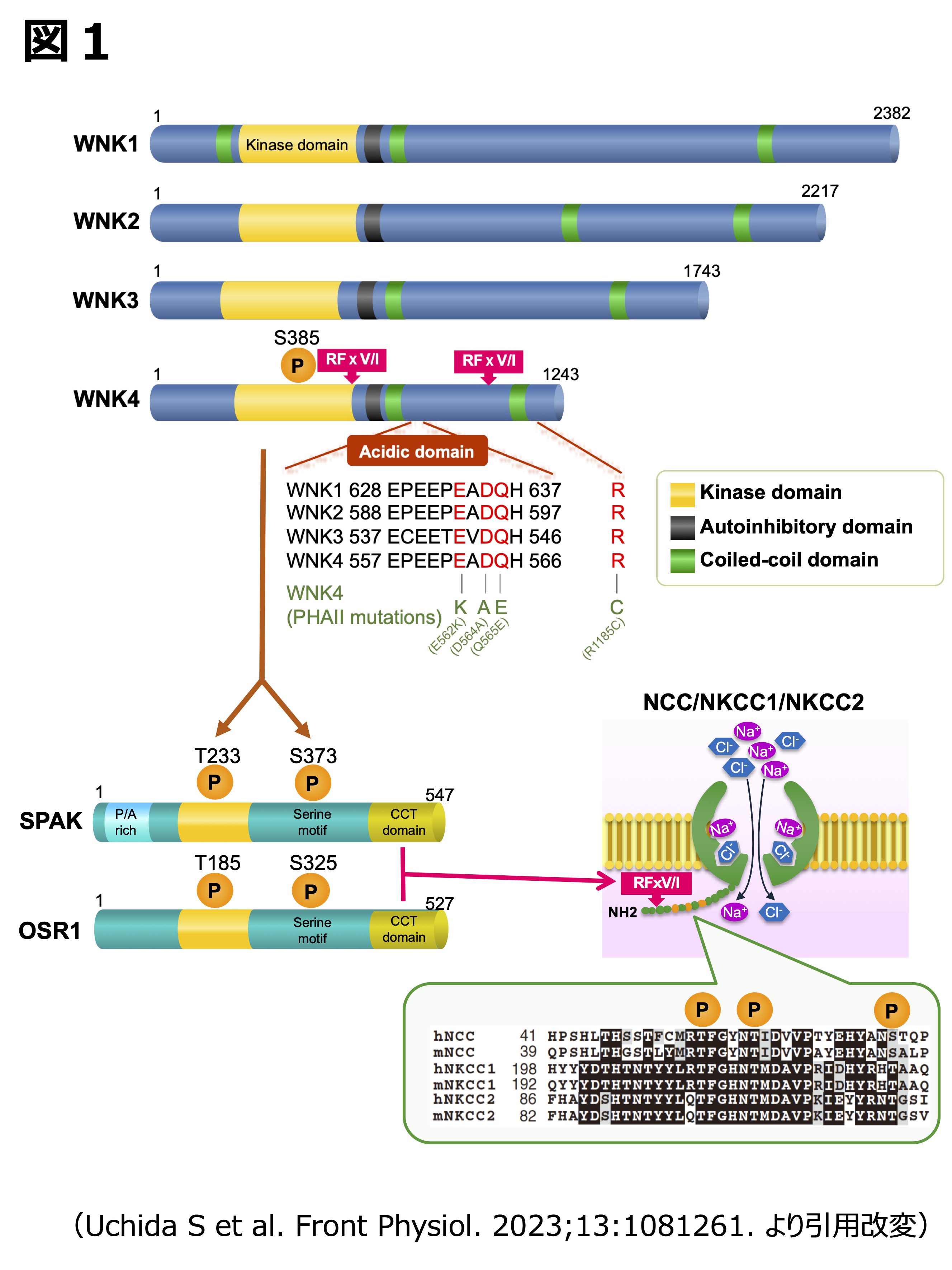
WNKキナーゼはセリン・スレオニンキナーゼファミリーの一つであり、キナーゼのcatalyticドメイン中に保存されているリジン(K)残基がシステイン(C)に置き換わっていることから With No Lysine (K) キナーゼと命名されました。哺乳類ではWNK1–4までのアイソフォームが知られており、図1に示すようにN末端側にキナーゼドメインを、その近傍にこれら4つのアイソフォーム間で相同性の高いアシディックドメインを持つ構造をとっています。
当初海外の他のグループから、アフリカツメガエル卵母細胞にWNKとNCCを強制発現させることでWNKの生理機能を検討する実験が数多く行われ、WNK4は生理的にNCCの機能を抑制するが、WNK4変異によってその抑制がはずれNCC機能亢進を招くという「負の調節因子(negative regulator)」説が通説となっていました。しかしながら強制発現実験の結果のみに依存するもので、内田研究室では学術的妥当性について懸念を持っていました。
2. WNK-OSR1/SPAK-SLC12A輸送体シグナルの発見
2005年にWNK1とWNK4の基質としてoxidative stress-responsive gene 1 (OSR1)とSte20-related proline-alanine-rich kinase(SPAK)が同定されました(図1)2), 3)。OSR1とSPAKのCCTドメインは、WNKキナーゼ内、及びNCCなどのSLC12A輸送体内のいずれにも存在する特定のアミノ酸配列(RFxV/I モチーフ)と親和性が高いことが報告され、すなわちNCCがOSR1とSPAKの基質であると推察されました。
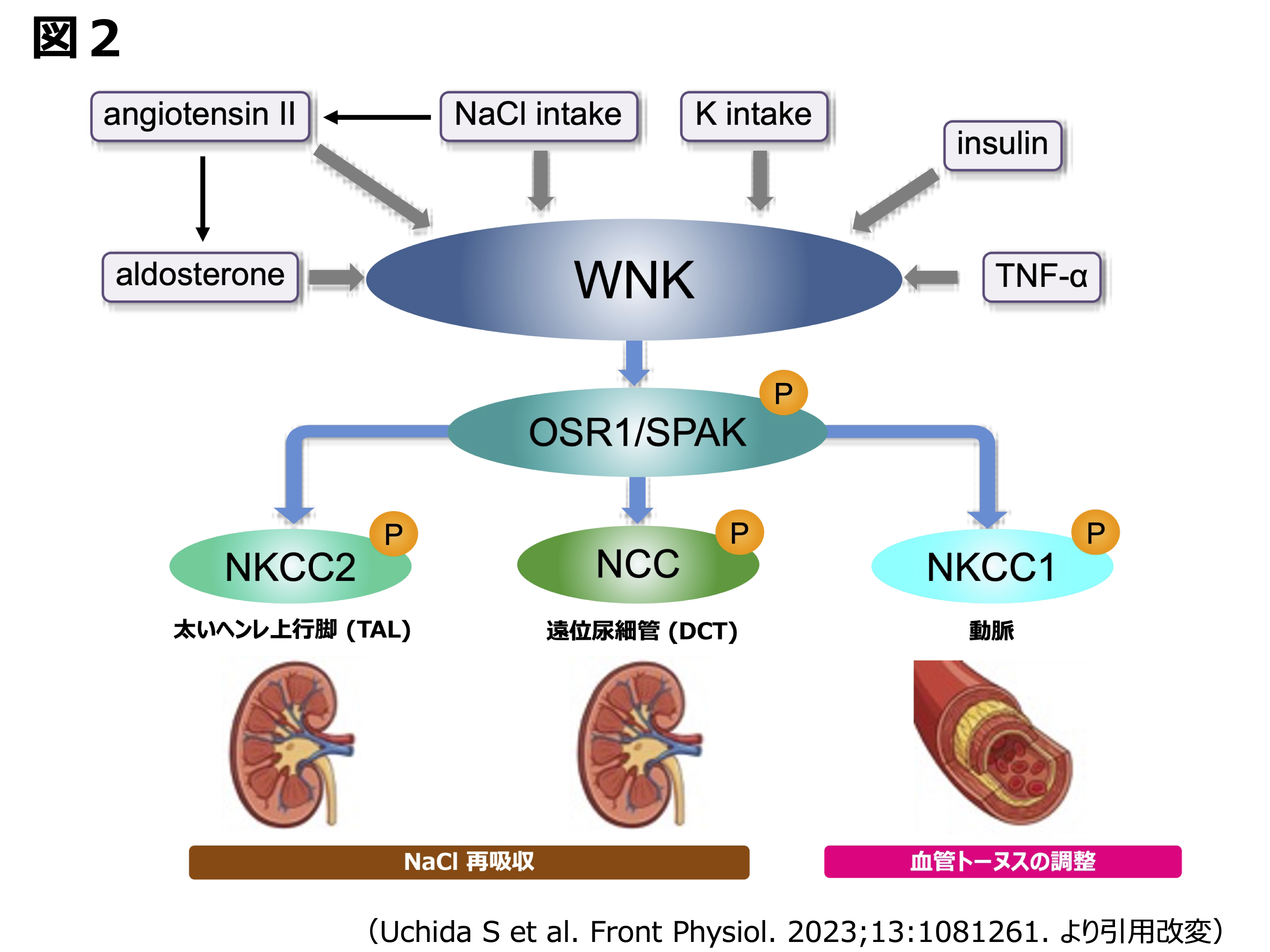
内田研究室ではPHAIIのモデルであるWNK4D561A/+変異ノックインマウスを世界に先駆けて作成し、高血圧、高カリウム血症、代謝性アシドーシスなど、PHAIIと同じ表現型を呈することを確認しました。さらに腎臓ではOSR1/SPAKのリン酸化亢進、およびNCCの発現量増加・輸送体機能の活性化を捉え、2007年にCell Metabolism 誌に報告しました4)。続いて、このマウスとSPAKとOSR1の不活化ノックインマウス[キナーゼ活性を減弱させる変異を導入したマウス SPAK(T243A) / OSR1(T185A)]を交配することにより、WNK4変異によるWNKキナーゼのNCCに対する活性化シグナルは、SPAKおよびOSR1に依存していることを報告しました5)。さらに当研究室ではWNK4 hypomorphic マウス(WNK4キナーゼ活性を減弱させたノックインマウス)6)、そしてWNK4ノックアウトマウスではSPAKの抑制に加え、NCCの発現が強く抑制されていることが確認できました7)。逆にWNK4過剰発現マウス(高コピートランスジェニックマウス)ではOSR1/SPAKおよびNCCの発現が顕著に亢進していました8)。このことからWNK4はOSR1/SPAKのリン酸化・活性化を経てNCCを活性化するという、WNK-OSR1/SPAK-NCCカスケードを形成していることが全てin vivoのデータで示されました(図2)。このことは、WNK4がNCCに対する正の制御因子(positive regulator)であることの証明となり、これまで台頭していたWNK4 negative regulator説を学術的に覆す結果となりました。
3. WNKシグナルの生理的意義とさまざまな制御因子
このシグナルは食事中の塩分量によって制御される(高塩では抑制・低塩では活性化)ことに加え、PHAII病態モデルノックインマウス(WNK4D561A/+)では高塩にしても抑制がかからず恒常的に活性化していることが判明し、このことがPHAⅡで持続的にNa再吸収が増加し、高血圧をきたす原因になっていると考えられました9)。
WNKシグナル発見以来、生理的な修飾因子について様々な検討が行われてきましたが、重要な刺激のひとつにアルドステロンがあることを我々は報告しています9)。尿細管におけるアルドステロンの作用系で既に知られているENaC(上皮型ナトリウムチャネル)に加えて、作用系の一端を担っていることが確認できました。同様に血圧を上昇させる方向に働くホルモンであるアンギオテンシンIIも、WNKシグナルを正に制御していることを確認しました10)。また細胞外カリウム濃度が直接WNK1活性を制御していることも培養細胞を用いた検討で確認しました11)。これらの制御因子に加え、一見血圧や塩分出納と無関係のようにみえるインスリンが実はWNKシグナルの強力な活性化因子であることも明らかにしています12), 13)。メタボリック症候群に代表される高インスリン血症ではこのWNKシグナルが恒常的に活性化され、肥満患者における塩分感受性高血圧の一因として重要な知見だと考えられました。
4. KLHL3・Cullin3によるWNKシグナル制御メカニズムの解明
次世代シークエンサー(NGS)を用いた未解決のPHAII家系解析によって、新たにKLHL3とCullin3 の変異が原因として発見されました14), 15)。これまでKLHL蛋白の一部はユビキチンE3リガーゼであるCullin3と結合し、ユビキチン化に関与することが知られていましたが、これら二つの遺伝子変異がWNKシグナルにどのような影響を与え、PHAIIの表現系を呈すのか、そのメカニズムは不明でした。
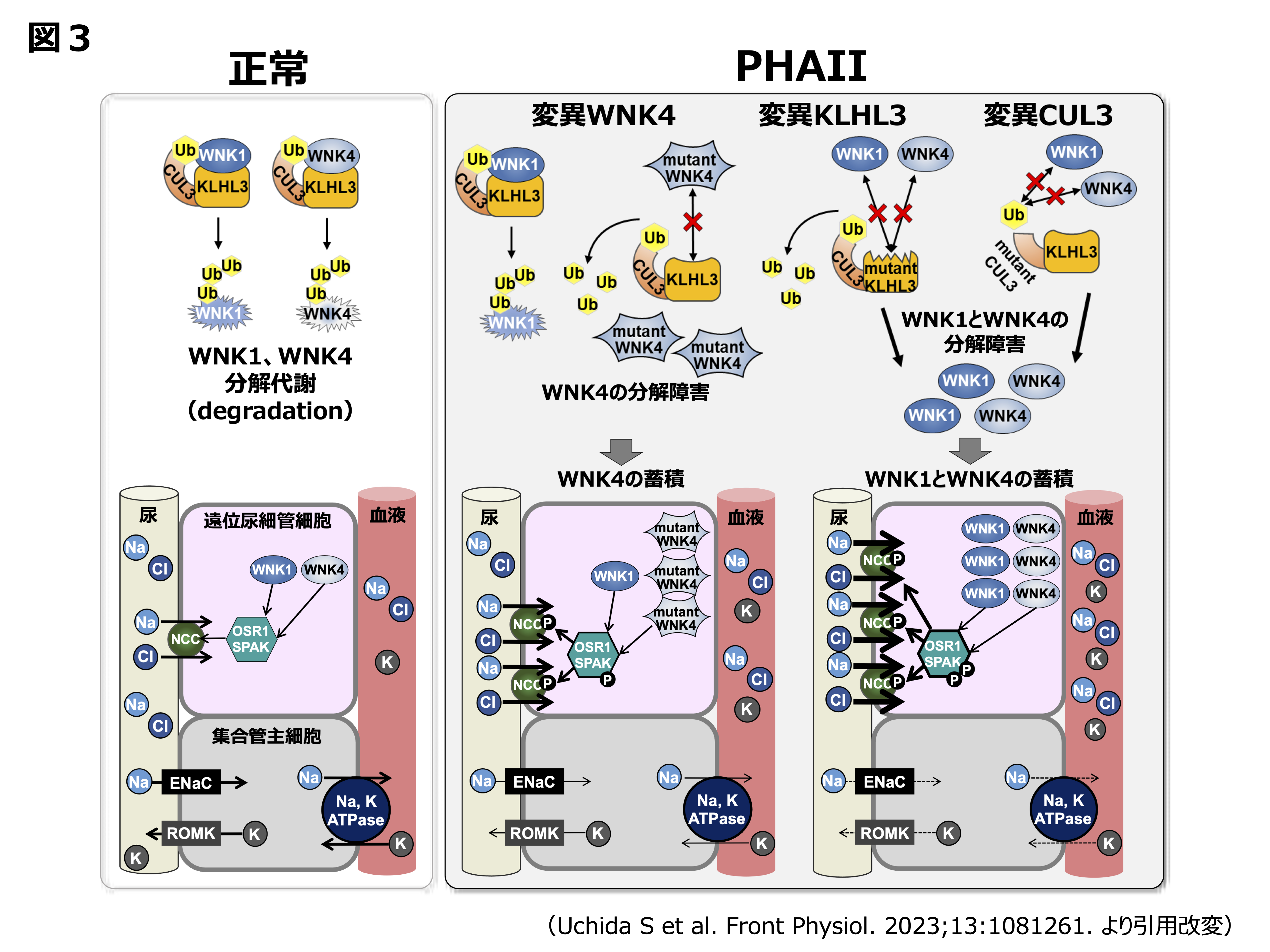
PHAIIを引き起こすKLHL3変異はKelchリピート・プロペラ構造の中央付近に集簇しており、何らかの基質蛋白との結合不全から、基質分解障害を招き、疾患発症に関与しているものと推定されました。WNKシグナルがOSR1/SPAKを介してNCCを強力に制御していることはこれまでの我々の研究から明らかであったため、まずKLHL3の基質を探索すべく、WNKシグナル各分子へ着目しました。免疫沈降実験によるアプローチにより、WNK4がその基質であることを明らかにしました8)。その後細胞実験、in vitro実験による詳細な検討により図3に示すようにCullin3-KLHL3は結合し、WNK4を基質としたユビキチンE3リガーゼ複合体を形成し、WNK4の分解制御に関わっていることが判明しました。PHAIIでみられた変異は、Cullin3, KLHL3, WNK4いずれも複合体形成不全を惹起するもので、WNK4の分解不全からWNK4蛋白の発現量増加をもたらすことに帰着することを明らかにしました。さらにKLHL3変異によるPHAII患者と同じ変異を導入したKLHL3変異ノックインマウスを作成・解析することで、実際に生体内でWNK1, WNK4の発現量増加が起こっていることも確認しました16)。
5. 血管収縮におけるWNKキナーゼの役割
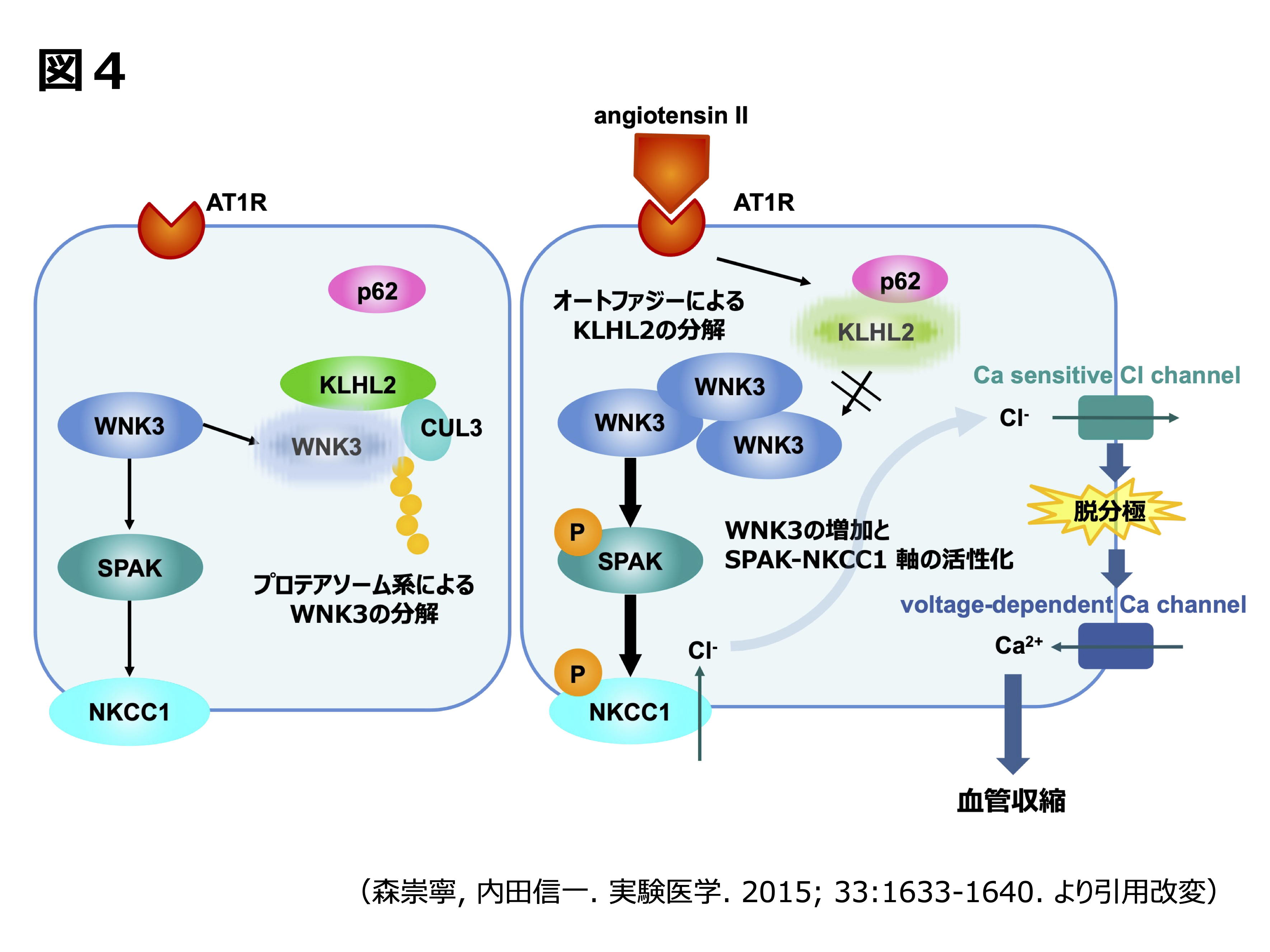
血圧・腎疾患の報告はありませんでしたが同じWNKファミリーに属するWNK3の生理機能を解明すべく、当研究室ではWNK3ノックアウト(KO)マウスを作成し解析を行いました。腎臓での表現系は確認されませんでしたが17)、このマウスに低塩食を与えた際に血圧が低下するという現象が観察されました。このことから腎臓以外、おそらく血管トーヌスにWNKシグナル(WNK3)が関与している可能性が想起されました。WNK3-KOマウスを解析することで、塩分摂取およびアンギオテンシンIIがWNK3-SPAK-NKCC1 リン酸化シグナルを制御し、血管緊張度(トーヌス)調節に関与していることを明らかにしました18)。さらに、KLHL3と極めて相同性の高い同じKLHLファミリーに属するKLHL2に着目し、KLHL3と同様WNKキナーゼの制御に関わる事を確認していたことから19)、血管におけるアンギオテンシンIIによるWNKシグナル活性化にKLHLが関与しているかどうかを検討しました。マウス大動脈と血管平滑筋細胞にはKLHL3ではなくKLHL2のみが発現しており、塩分制限およびアンギオテンシンII負荷によりKLHL2の減少、WNK3の増加が確認されました。ノックダウン実験によりこのシグナルはKLHL2及びWNK3に依存していることを確認し、またKLHL2の減少にはp62 (SQSTM1)を介したオートファジーが関与していることを報告しました18)(図4)。アンギオテンシンIIによる血管トーヌス制御メカニズムにKLHL2-WNK3-SPAK-NKCC1シグナルカスケードが関与することを示し、生理学的にも意義のある知見となりました。
6. WNK4脂肪分化への関与、創薬・バイオマーカー創出への挑戦
このように当教室では、WNKシグナルは血圧や塩分出納調節に重要な役割を果たし、様々な制御因子により調節されていることを示し報告してきました。さらにWNKシグナルは血圧制御系に限定されず、当研究室では脂肪細胞にWNK4が発現していること、WNK4-KOマウスが健康的に痩せていることに着目し脂肪細胞の解析を行うことで、WNK4が脂肪形成促進因子である可能性を見出し、報告しました20)。これらの知見を踏まえると、WNKシグナルは新規降圧利尿薬、抗肥満薬として新規創薬ターゲットとしての可能性を有すると期待されました。当研究室ではWNKシグナル遮断薬スクリーニングを実施すべく蛍光相関分光法を用いたWNK-SPAK結合阻害薬ハイスループット・スクリーニング系21)、ELISAを用いたSPAK直接阻害薬検出系を確立し、in vivoでWNKシグナル阻害活性を示す複数の有望化合物同定に成功しています22)。
さらにWNKシグナルの活性化評価のバイオマーカーとして、ELISAによる尿中リン酸化NCCの定量検出法を確立しました23)。この検査法は患者侵襲が低い上、WNKシグナル活性評価にとどまらず、Gitelman症候群やPHAII患者のようなNCC活性に変化を来す遺伝性腎疾患のスクリーニングにも有用で、事実Gitelman患者では著明な減少、PHAII患者では著明な上昇をきたしていることを確認しています23)。
おわりに
内田研究室では、単一遺伝子異常から高血圧を呈するWNKキナーゼに着目し、10余年にわたる真摯な探求を続けてまいりました。その歩みは、稀少疾患であるPHAIIの病態解明にとどまらず、腎臓における電解質代謝調節の基盤となる数多くの生理学的知見を世に問うものでした。 特筆すべきは、当時の学界において支配的であった「WNK=負の調節因子(negative regulator)」説という潮流に迎合することなく、一貫して科学的真実を追求し続けられた点にあります。結果として、現在の定説である「正の調節因子(positive regulator)」理論を確立するに至ったその軌跡は、内田先生が背中で示し続けてこられた「信念を曲げずに研究に邁進することの重要性」を、何よりも雄弁に物語っています。本項が、内田研究室の真理探究の精神を次代へと繋ぐ一助ともなれば幸いです。
1. Wilson FH, Disse-Nicodème S, Choate KA, et al. Human hypertension caused by mutations in WNK kinases. Science. Aug 2001;293(5532):1107-12. doi:10.1126/science.1062844
2. Moriguchi T, Urushiyama S, Hisamoto N, et al. WNK1 regulates phosphorylation of cation-chloride-coupled cotransporters via the STE20-related kinases, SPAK and OSR1. J Biol Chem. Dec 2005;280(52):42685-93. doi:10.1074/jbc.M510042200
3. Vitari AC, Deak M, Morrice NA, Alessi DR. The WNK1 and WNK4 protein kinases that are mutated in Gordon's hypertension syndrome phosphorylate and activate SPAK and OSR1 protein kinases. Biochem J. Oct 2005;391(Pt 1):17-24. doi:10.1042/BJ20051180
4. Yang SS, Morimoto T, Rai T, et al. Molecular pathogenesis of pseudohypoaldosteronism type II: generation and analysis of a Wnk4(D561A/+) knockin mouse model. Cell Metab. May 2007;5(5):331-44. doi:10.1016/j.cmet.2007.03.009
5. Chiga M, Rafiqi FH, Alessi DR, et al. Phenotypes of pseudohypoaldosteronism type II caused by the WNK4 D561A missense mutation are dependent on the WNK-OSR1/SPAK kinase cascade. J Cell Sci. May 2011;124(Pt 9):1391-5. doi:10.1242/jcs.084111
6. Ohta A, Rai T, Yui N, et al. Targeted disruption of the Wnk4 gene decreases phosphorylation of Na-Cl cotransporter, increases Na excretion and lowers blood pressure. Hum Mol Genet. Oct 2009;18(20):3978-86. doi:10.1093/hmg/ddp344
7. Takahashi D, Mori T, Nomura N, et al. WNK4 is the major WNK positively regulating NCC in the mouse kidney. Biosci Rep. 2014;34(3)doi:10.1042/BSR20140047
8. Wakabayashi M, Mori T, Isobe K, et al. Impaired KLHL3-mediated ubiquitination of WNK4 causes human hypertension. Cell Rep. Mar 2013;3(3):858-68. doi:10.1016/j.celrep.2013.02.024
9. Chiga M, Rai T, Yang SS, et al. Dietary salt regulates the phosphorylation of OSR1/SPAK kinases and the sodium chloride cotransporter through aldosterone. Kidney Int. Dec 2008;74(11):1403-9. doi:10.1038/ki.2008.451
10. Talati G, Ohta A, Rai T, et al. Effect of angiotensin II on the WNK-OSR1/SPAK-NCC phosphorylation cascade in cultured mpkDCT cells and in vivo mouse kidney. Biochem Biophys Res Commun. Mar 2010;393(4):844-8. doi:10.1016/j.bbrc.2010.02.096
11. Naito S, Ohta A, Sohara E, et al. Regulation of WNK1 kinase by extracellular potassium. Clin Exp Nephrol. Apr 2011;15(2):195-202. doi:10.1007/s10157-010-0378-9
12. Sohara E, Rai T, Yang SS, et al. Acute insulin stimulation induces phosphorylation of the Na-Cl cotransporter in cultured distal mpkDCT cells and mouse kidney. PLoS One. 2011;6(8):e24277. doi:10.1371/journal.pone.0024277
13. Nishida H, Sohara E, Nomura N, et al. Phosphatidylinositol 3-kinase/Akt signaling pathway activates the WNK-OSR1/SPAK-NCC phosphorylation cascade in hyperinsulinemic db/db mice. Hypertension. Oct 2012;60(4):981-90. doi:10.1161/HYPERTENSIONAHA.112.201509
14. Boyden LM, Choi M, Choate KA, et al. Mutations in kelch-like 3 and cullin 3 cause hypertension and electrolyte abnormalities. Nature. Feb 2012;482(7383):98-102. doi:10.1038/nature10814
15. Louis-Dit-Picard H, Barc J, Trujillano D, et al. KLHL3 mutations cause familial hyperkalemic hypertension by impairing ion transport in the distal nephron. Nat Genet. Apr 2012;44(4):456-60, S1-3. doi:10.1038/ng.2218
16. Susa K, Sohara E, Rai T, et al. Impaired degradation of WNK1 and WNK4 kinases causes PHAII in mutant KLHL3 knock-in mice. Hum Mol Genet. Oct 01 2014;23(19):5052-60. doi:10.1093/hmg/ddu217
17. Oi K, Sohara E, Rai T, et al. A minor role of WNK3 in regulating phosphorylation of renal NKCC2 and NCC co-transporters in vivo. Biol Open. Feb 2012;1(2):120-7. doi:10.1242/bio.2011048
18. Zeniya M, Morimoto N, Takahashi D, et al. Kelch-Like Protein 2 Mediates Angiotensin II-With No Lysine 3 Signaling in the Regulation of Vascular Tonus. J Am Soc Nephrol. Sep 2015;26(9):2129-38. doi:10.1681/ASN.2014070639
19. Takahashi D, Mori T, Wakabayashi M, et al. KLHL2 interacts with and ubiquitinates WNK kinases. Biochem Biophys Res Commun. Aug 02 2013;437(3):457-62. doi:10.1016/j.bbrc.2013.06.104
20. Takahashi D, Mori T, Sohara E, et al. WNK4 is an Adipogenic Factor and Its Deletion Reduces Diet-Induced Obesity in Mice. EBioMedicine. Apr 2017;18:118-127. doi:10.1016/j.ebiom.2017.03.011
21. Mori T, Kikuchi E, Watanabe Y, et al. Chemical library screening for WNK signalling inhibitors using fluorescence correlation spectroscopy. Biochem J. Nov 01 2013;455(3):339-45. doi:10.1042/BJ20130597
22. Kikuchi E, Mori T, Zeniya M, et al. Discovery of Novel SPAK Inhibitors That Block WNK Kinase Signaling to Cation Chloride Transporters. J Am Soc Nephrol. Jul 2015;26(7):1525-36. doi:10.1681/ASN.2014060560
23. Isobe K, Mori T, Asano T, et al. Development of enzyme-linked immunosorbent assays for urinary thiazide-sensitive Na-Cl cotransporter measurement. Am J Physiol Renal Physiol. Nov 01 2013;305(9):F1374-81. doi:10.1152/ajprenal.00208.2013
